医師の画像診断業務を効率化する画像位置合わせ機能の開発
1.はじめに
1.1 我が国における画像診断医の現状
医療分野における画像診断とは,主に放射線科診断専門医の資格を持った医師(以下,画像診断医)が,CT,MRI装置で撮影した医用画像を用いて,疾患の有無(存在診断)や種類(質的診断),進行段階(病期診断)などを診断する行為を一般に指す.
我が国における画像診断の現状は,数多くのCT,MRI装置と,少ない画像診断医によって特徴付けられる1).日本は人口あたりのCT,MRI装置の設置台数が2016年現在世界1位2)であり,年間検査回数は約3,400万件以上に及ぶ3).しかし,そのうち画像診断医により画像診断が行われ,診断報告書が作成された割合は4割程度と推定される3).これは,CT,MRI装置の多くが画像診断医の常勤しない施設に設置されているためといわれている1).
問題なのは,単に画像診断医の不足だけではなく,近年の撮影装置の高度化により,見るべき画像枚数が膨大になっている点である.たとえば,肺結節と呼ばれる直径数mmの小さな腫瘍を見つけるため,厚み1mm以下の断面画像(以下,スライス)を高画質で撮影できるようになったが,1回の検査で数百~千枚程度のスライスが発生するケースが出てきている.このため,画像診断医の業務負荷がますます増えている.

1.2 医療現場に浸透しつつあるコンピュータ支援診断
画像診断医の業務負荷増大の問題に対して,コンピュータ支援診断(Computer Aided Diagnosis : CAD)の活用が進んでいる.すでに,存在診断を目的としたコンピュータ支援検出 (Computer Aided Detection : CADe) が,乳がんや肺がんの検診等に導入され始めている4),5).一方,良悪性鑑別などの質的診断を目的としたシステムはCADeと区別するため,CADxと呼ばれ,多くは研究段階ではあるが,今後,臨床適用が期待される6),7).なお,これ以外にも画像所見の自動生成8)や類似症例検索9),10),11),腫瘍サイズの自動計測12)といったさまざまな形態で画像診断に資する情報を取得・提示するCADも研究開発が進んでいる.
国内CAD市場では,2014年薬事法改正により,これまで,医療機器として常にハードウェアとの一体販売が必要であった医療用ソフトウェアが単独で流通可能となった.これにより, CADを含む診断支援ソフトウェア単体製品の市場規模は2013年の12億円から今後急速に拡大が見込まれ,2020年には175億円に達すると見込まれている13).研究用途が中心であったCADが,いよいよ臨床の現場にも普及し始めている.
1.3 本研究の目的と本稿のねらい
CADは画像診断医の見落としや思い込みなどのヒューマンエラーに対するフォローや,ダブルチェックによる診断の確信度向上といった診断精度を高める目的で主に利用される.これに対し,本研究で目指すのは画像診断医がすぐに診断に取りかかれるように,たとえばある患者の過去画像と現在画像の表示位置を揃えておくといった準備作業を自動化し,診断業務を効率化することである.
本稿は,医用画像解析の技術開発で求められる要件や検討すべき項目,そして,これから本分野に取り組まれる読者にとって有益となる情報をできるだけ多く織り交ぜた.第2章では事前検討として,画像診断の業務分析を行い,画像位置合わせの自動化による業務効率化の仮説と,要件定義について述べる.第3章では,画像位置合わせの実現方法について,技術的な観点から述べる.第4章では開発方式の性能評価と,医療現場での業務効率化の検証結果を述べる.最後に,筆者らの知見に基づき,医用画像解析の技術開発を始める際に知っておきたい知識や考え方などについて第5章で述べる.
2.事前検討
本章では画像診断業務の支援方法を考えるために,まず現状の業務フローを把握した上で(2.1節),どの部分を効率化すべきか(2.2節),そして,その効率化にはどういった機能で応え,どれくらいの性能を満たすべきか(2.3節),検討したことを述べる.
2.1 業務分析
一般的な診察~画像診断の業務フローと現場の様子をそれぞれ図1,図2に示す.たとえば,主治医が患者を診察し,胸部CT検査が必要と判断したとする.主治医は検査依頼を放射線科情報システム(Radiology Information Systems : RIS)へ送る.RISから依頼を受け取ったCT室の診療放射線技師は,患者受付,装置の操作,モニタリング,画像処理などを行い,撮影画像を画像保管通信システム(Picture Archiving and Communication System:PACS)へ送る.読影室にいる画像診断医は, RISから送られた診断依頼の一覧から患者を選び,対象患者の撮影画像をPACSから取得する.取得した画像を参照し,その結果を主治医に伝えるために診断報告書を作成する.
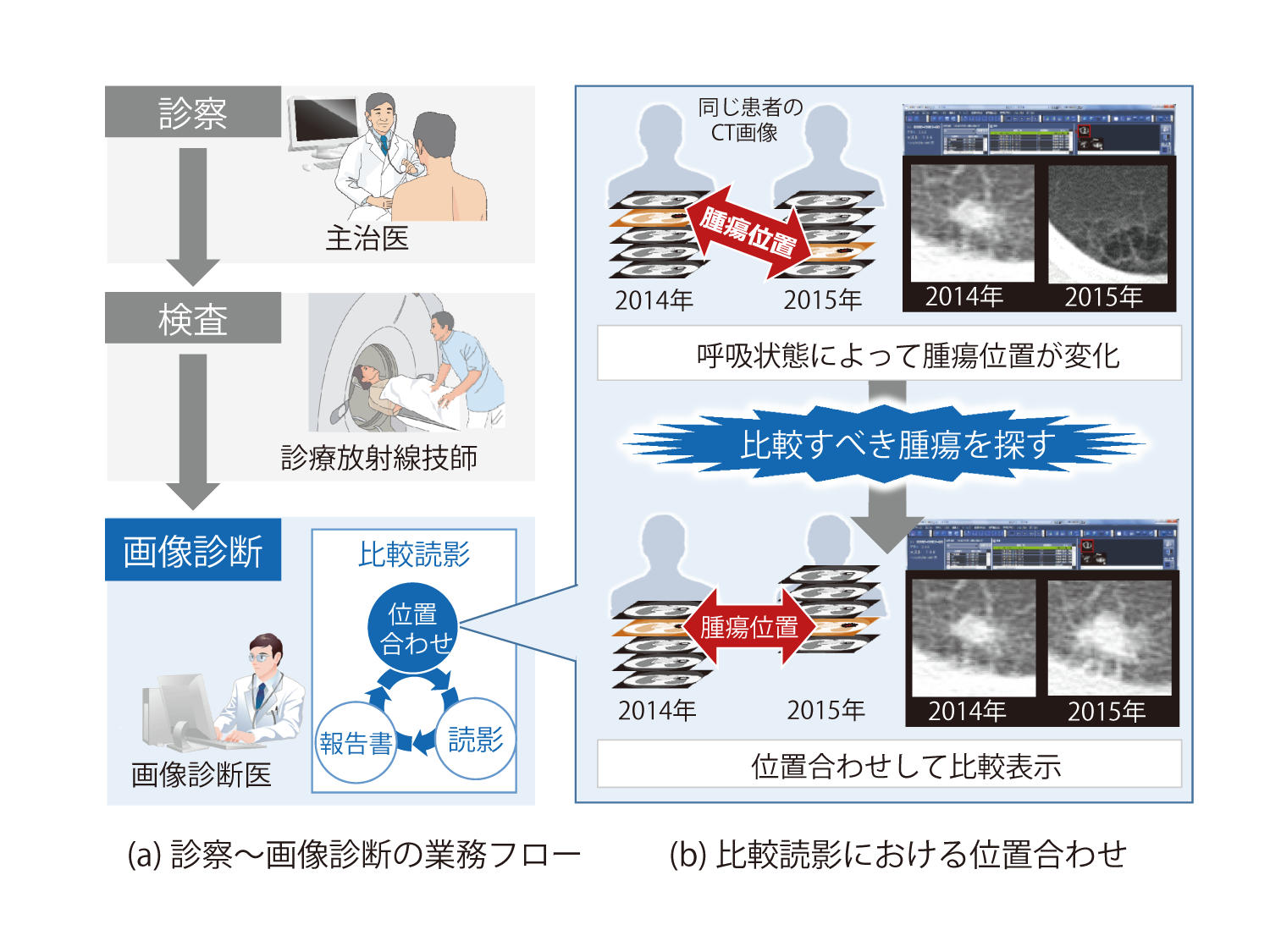

以下,画像診断業務に着目し,より詳しい業務分析を行った結果について述べる.CTがん検診などの画像診断の業務においては,ある一時点の画像からは腫瘍の質的診断が難しい場合があり,経過観察として数週間~数カ月の間隔を空けて撮影した複数時点の画像を見比べること(以下,比較読影)で,腫瘍の時間変化を観察し,診断を行っている14).
比較読影では,前回の画像撮影時に見つかった腫瘍と,今回撮影した画像の腫瘍を見比べるため,画像位置合わせにより患者の体位や呼吸・心拍による3次元の変動を補正する必要がある.現状は,手作業で比較すべき腫瘍を探しており,1回の作業で数秒~数十秒かかっている(図 1(b)).次に,腫瘍の大きさ・形状・濃度等の時間変化を観察し,良悪性の鑑別や疑いのある疾患名を洗い出す作業(以下,読影)を行う.最後に,その読影結果を診断報告書に記載する.
2.2 業務効率化の対象
今回調査に協力いただいた医療施設では,検査を行ったその日のうちに結果を患者へ説明する即時読影を実現している.そのため,効率的な画像診断が要求されている.たとえば,マウス操作時間の短縮のため,多機能マウスを利用した各種機能のショートカット割当てや,キーボードの入力時間短縮のために音声入力を活用するなど,極力,ルーチンワークを省力化する工夫がされている(図 2 (c)).
さらなる画像診断業務の効率化を目指し,コンピュータ支援の方法を考える.たとえば,腫瘍を自動で検出できるCADeを用いて,あらかじめ診断対象となる候補を絞り込むことができれば,画像診断医は見るべき画像枚数が減り,業務効率化が期待できる(図3 (a)).しかし,コンピュータの処理結果だけを見て判断したとすると,CADeの性能によっては検出漏れが発生する可能性がある.このため,国内で医療機器認定されているCADeは,腫瘍検出といった正解が何個あるか分からない課題を扱う場合,画像診断医が最初に全数チェックを行い,その後,CADeの結果を確認する運用(図 3 (b))となっている15).
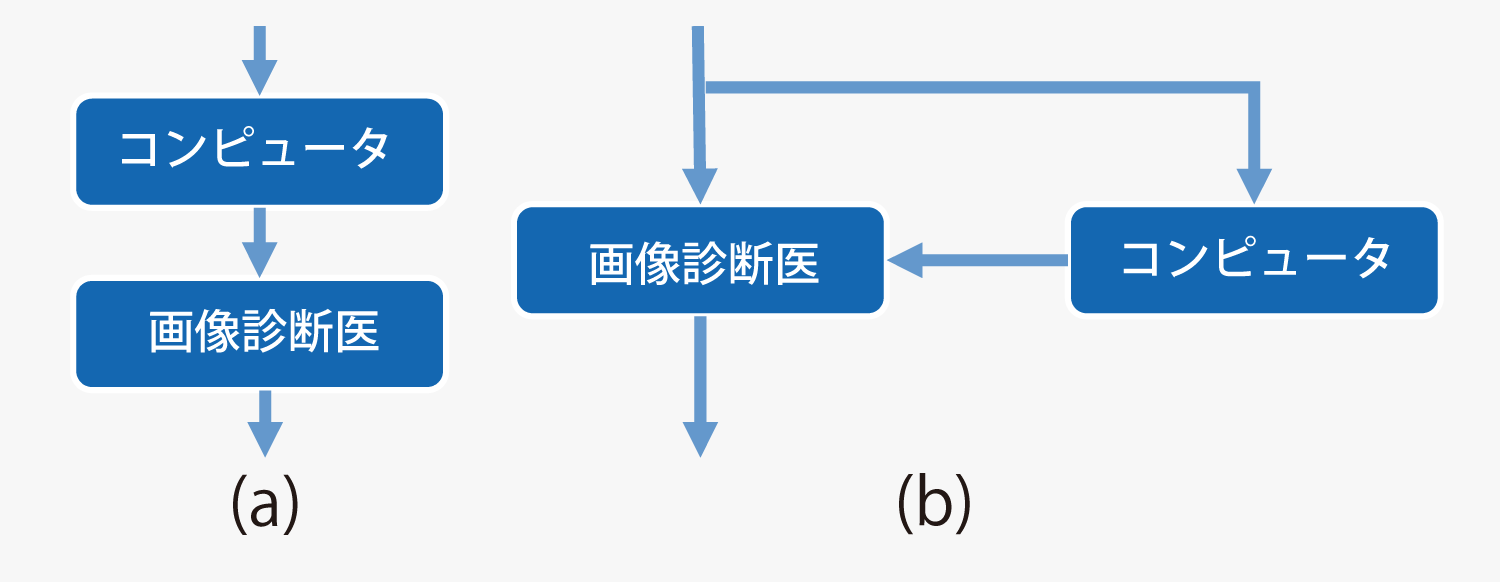
一方,比較読影時のルーチンワークの1つである画像位置合わせの自動化といった課題であれば,正解が必ず1つしかないので,図 3(a)のように画像診断医はその処理結果を見て,正誤を判断するだけでよい.仮に処理結果に誤差があったとしても,その処理結果の位置から周辺に向かって画像を参照しながら,正解となる画像位置を探して行けばよいので,画像診断医は全数チェックとなることはない.
したがって,本研究では画像診断業務の効率化に直接貢献が期待できる画像位置合わせ作業の自動化を目指す.
2.3 要件定義
A. 機能要件
経過観察時の比較読影の業務フローを踏まえて,本研究の画像位置合わせを,“比較する2組の検査画像において,一方の画像上で画像診断医が指定した関心領域(Region of Interest : ROI)に対応する他方の画像上の3次元位置を求めること”と定義する.経過観察時の比較読影では,たとえば過去画像にて腫瘍領域がROIとしてすでに決まっているため,そのROIの現在画像における対応位置を求めることで腫瘍の定点観察を実現したい.
画像位置合わせ結果の提示方法は,全画素位置を合わせる非剛体変形ではなく剛体変形(本研究では拡大縮小と平行移動のみ)とした.CTがん検診などの経過観察時の比較読影では,腫瘍の最大径を計測して経時変化を見ることがある.このとき,画像を歪ませる非剛体変形は,画像診断医にとってアーチファクト(誤診の原因)と見なされることがあるため剛体変形を選択した.ただし,実際には非剛体変形が起きているため,ROIの中心点が比較画像間で揃っていることを機能要件とした.
B. 精度
肺がんCT検診ガイドライン14)によれば経過観察の対象となる腫瘍サイズは最大径6mm以上である.最も高い画像位置合わせ精度が求められるケースは,最小サイズの腫瘍を内包する6mm四方のROIを設定し,ROI内の画像のみを画像位置合わせ結果として提示するケースである(図4(a)).この条件下で,仮に誤差が発生したとしても,画像位置合わせ後のROI内に少なくとも腫瘍の一部が確認できれば(図 4(b),(c)),画像診断医による正しい位置(図 4(a))への修正が容易に可能と考えた.
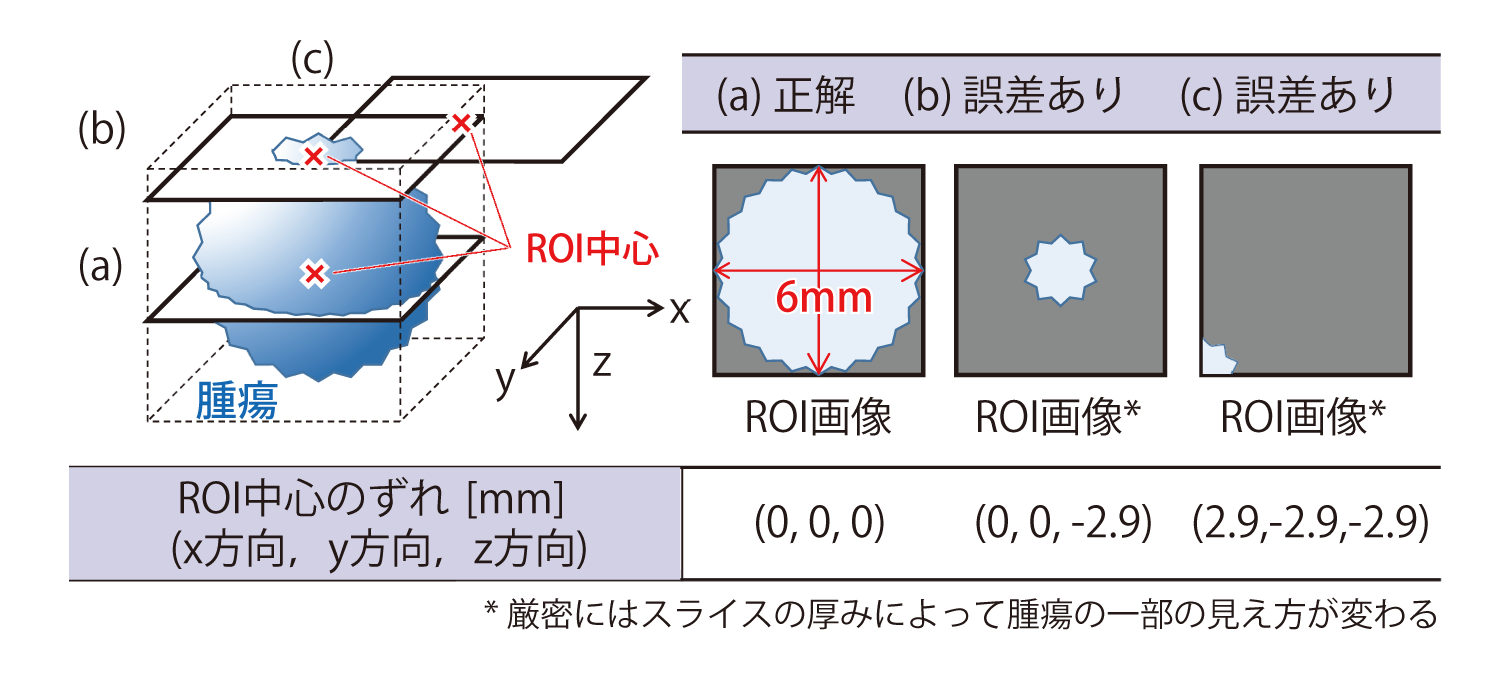
腫瘍の一部が目視で確認できる限界の誤差が,z方向に3mm未満(図 4(b))のときであり,ここからさらにxy各方向に最大3mm未満(図 4(c))まで許容できる.したがって,本研究では,目標精度を少なくともxyz各方向にそれぞれ誤差3mm未満(図 4の点線の立方体の内側)とした.
C. 処理時間
医用画像を含む医療情報をシステムで扱う上で,守るべきルールに“見読性・真正性・保存性の確保”(電子保存三原則)がある16).厚労省のガイドライン17)によれば,見読性の確保とは,電子媒体に保存された内容を,権限保有者からの「診察」,「患者への説明」,「監査」,「訴訟」などの要求に応じて,それぞれの目的に対し支障のない応答時間やスループットと操作方法で,肉眼で見読可能な状態にできることである.したがって,画像位置合わせ機能も画像診断業務の目的に対し,支障のない応答時間で画像位置合わせ結果を表示する必要がある.本研究では,思考阻害がなく受容可能な応答時間として2秒を目標に設定した.
次に,真正性の確保とは,正当な権限において作成された記録に対し,虚偽入力,書き換え,消去および混同が防止されており,かつ,第三者から見て作成の責任の所在が明確であることである17).特に画像情報に関しては,読影時に利用した状態で保存する必要があり,可逆圧縮画像にて診断を行った場合は,そのままの状態で保存し,非可逆圧縮による保存を行ってはならない取り決めがある18).
保存性の確保では,画像情報は医療法施行規則第20条で2年間,保険医療機関および保険医療養担当規則9条では完結の日から3年間の保存義務が発生する.一方で,過去画像の利用に目を向けると,2年を超える長期の経過観察が必要な場合もあることから14),法令が定める保管期間を過ぎても単純には画像を捨てられない実状がある.
以上を勘案すると,画像は可逆圧縮で長期保管が必要となるため,画像位置合わせ機能の搭載が想定されるPACSは,ストレージにかかるコストが大きい.目標とする応答時間を担保するために,事前に中間処理を行っておく方式もあるが19),中間処理結果を保持することで,ストレージコストがさらに増大してしまう欠点がある.したがって,画像位置合わせは事前処理なしで処理時間2秒を目指す.
3.画像位置合わせ機能の開発
3.1 基本方式
画像位置合わせの方式には,画素値を利用する輝度ベースと,特徴点周辺の特徴量を利用する特徴ベースの2通りがある.経過観察では比較画像間で腫瘍増大などの経時変化が起こる可能性があるため,部分的な画像変化に頑健な特徴ベースを採用した.図5に画像位置合わせの基本方式の処理フローを示す.
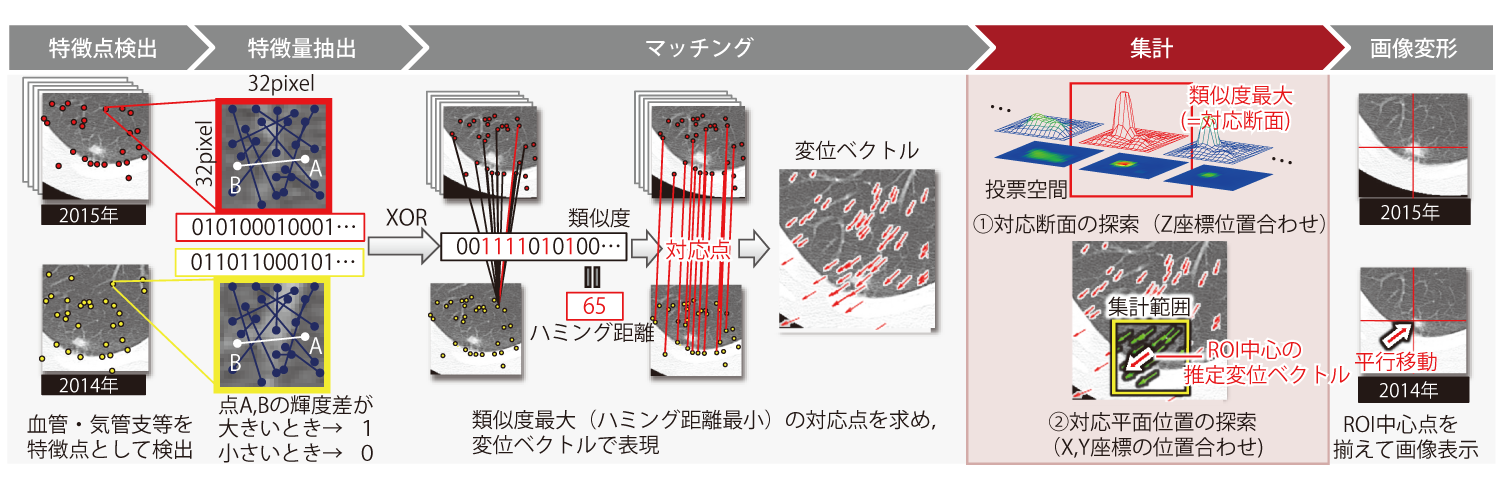
たとえば,比較元画像の腫瘍をROI指定した場合,そのROIの中心座標(x,y,z)を入力する.次にROI周辺から血管や気管支などを特徴点として検出し,特徴点近傍の輝度パターンをバイナリ表現した画像特徴量を抽出する.比較画像間で特徴点の画像特徴量を比較し,最も類似する(ハミング距離最小の)特徴点のペアを見つける.ROI中心からある一定範囲における各特徴点のペア(以下,変位ベクトル)を集計することで,ROI中心の変位ベクトル(dx,dy,dz)を推定し,画像位置合わせ結果として対応ROIの中心座標(x+dx,y+dy,z+dz)を出力する.比較読影用途では,この画像位置合わせ結果に基づき比較先画像を平行移動して,比較画像間でROI中心点の位置を揃えて表示する.
先述した集計方法について詳しく説明する.まず前処理としてマッチング結果から誤対応を除去する.次に,比較元画像のスライスに対応する比較先のスライス(z座標)を求めるため,比較先画像の各スライスの変位ベクトルを投票空間にマッピングし,投票値が最大となるスライスを求める.最後に,求めた対応スライスにおいて,ROI中心から一定距離の範囲で変位ベクトルをサンプリングし,平均化するとROI中心点の変位ベクトルが求まる.
3.2 技術課題
図 5集計の②対応平面位置の探索にて,集計範囲に含まれる変位ベクトルが少ないと画像位置合わせ精度が下がる課題がある.なぜなら,肺内は連続体であるので,本来はROI中心を取り囲むように変位ベクトル場があり,その各変位ベクトルの均衡が取れた結果としてROI中心の変位ベクトルが求まる.しかし,変位ベクトルが現れる血管や気管支は,肺内にまばらにしか存在していないため,集計範囲によっては観測される変位ベクトルが少なく,その分布に偏りが生じてしまうことがある(図6).

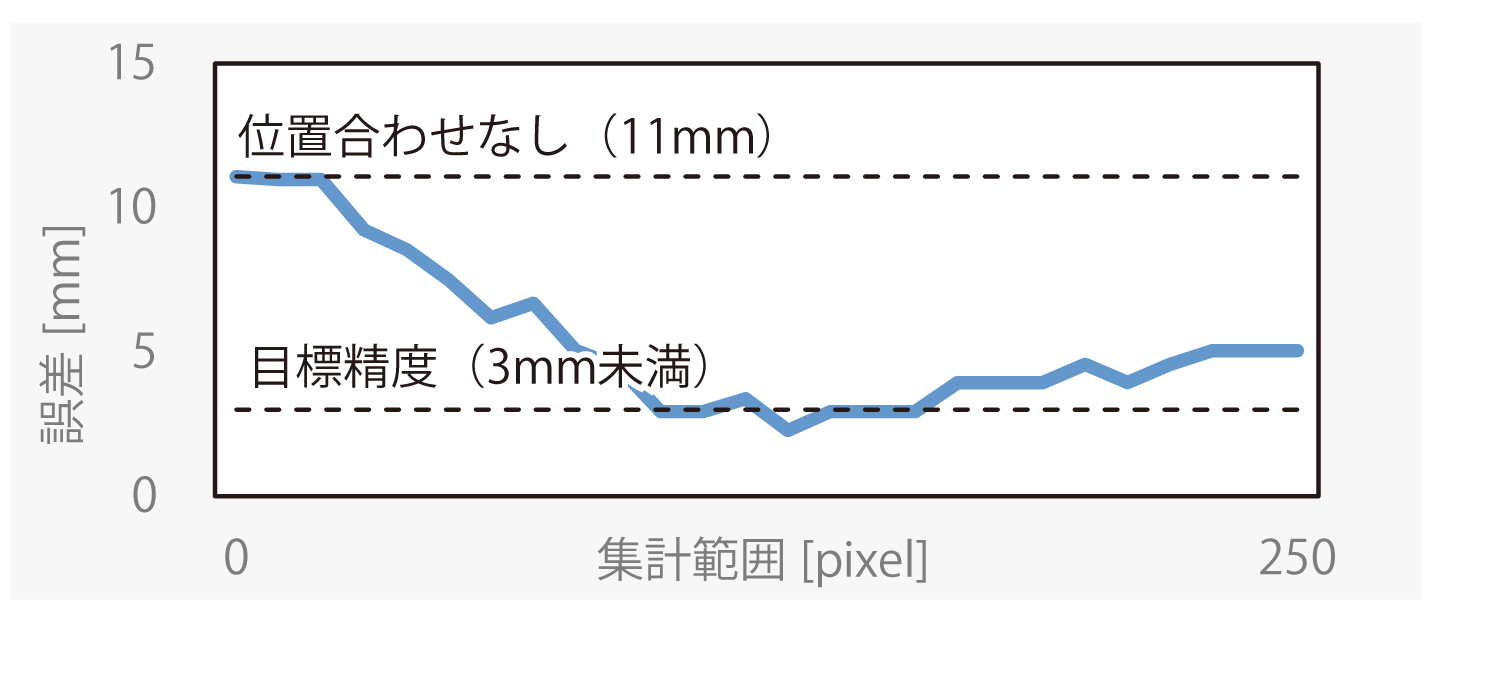
そこで,変位ベクトルを出来るだけ万遍なく集計しようと集計範囲を広げた場合,広げ過ぎによる画像位置合わせ精度の低下という新たな問題が起きることがある(図7).これは,ROI中心と異なる呼吸変動となる遠方の変位ベクトルも集計時に含んでしまうため,これが誤差を生む原因となる.なお,最適な集計範囲は常に一定ではなく,症例ごとに異なることが事前に分かっており,あらかじめ実験的に求めておくことができない.
3.3 開発方式:放射状特徴点サンプリング
我々はROIの高精度な画像位置合わせを実現するため,“放射状特徴点サンプリング”20)と呼ばれる変位ベクトルの最適な集計範囲とその集計方法を開発した.処理手順は下記の通り.
① ROI中心点と同心の扇形に領域を分割し,各領域にてROI中心に最も近い変位ベクトルを探索(図8(a))
② 見つけた最近傍の変位ベクトルとROI中心点との距離に応じた重み付け(たとえば,近いほど重みが増すように距離の逆数)を設定
③ 全領域の変位ベクトルを加重平均によりROI中心の変位ベクトルを推定(図 8 (b))
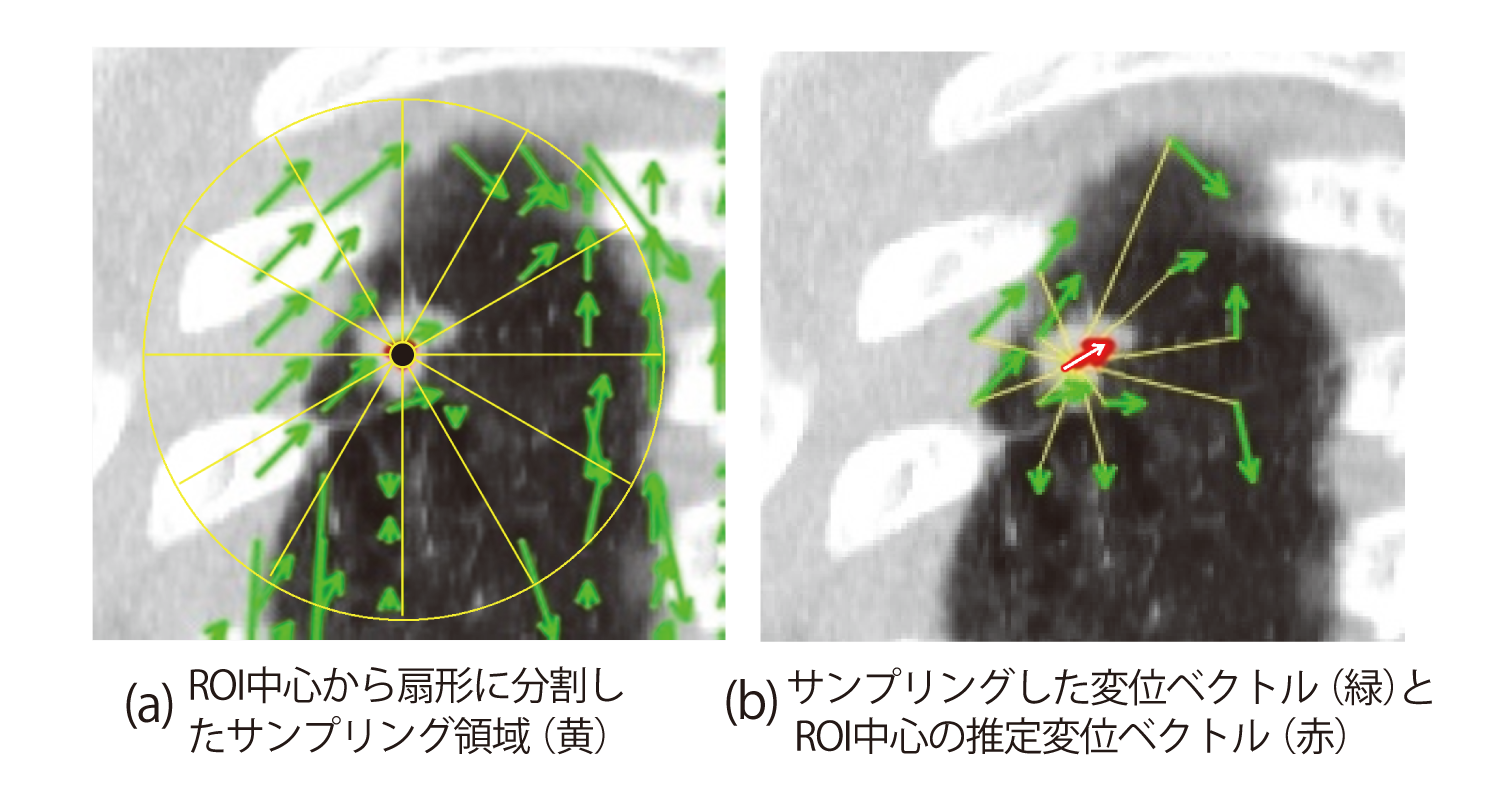
この方式の考え方を説明する.ROI中心の変位ベクトルはその周辺で起こる斥力・引力の合算により決定されると仮定すると,全方位から万遍なく変位ベクトルをサンプリングしてくる必要がある.しかし,実際には観測される変位ベクトルは,血管等の分布によって偏在しているので,遠方の変位ベクトルも含めて,全方位からできるだけ均等に変位ベクトルをサンプリングしてくる.遠方の変位ベクトルほどROI中心の変位ベクトルと異なる可能性が高くなるため,最近傍の変位ベクトルを集計するときに距離に反比例した重み付けを行うことで調整する.
4.評価
開発方式の目標性能に対する評価結果と,医療現場における業務効率化の検証結果について述べる.
4.1 性能評価
固定範囲で変位ベクトルを集計する基本方式と,集計方法に放射状特徴点サンプリングを採用した開発方式との精度比較を行った.また,開発方式の処理時間を計測した.
A. 評価用データおよび評価方法
肺がん患者5名の経過観察時の胸部CT画像を実験に用いた(表1).同一患者で異なる日時の2組の胸部CT画像を1症例とし,各症例に対して,体軸断(Axial),冠状断(Coronal),矢状断(Sagittal)の3方向 のスライスからなる合計15件のデータを評価した.

各データにて,一方の画像に写る腫瘍をROIとして設定した場合に,他方の画像に写る腫瘍の中心座標と求めた対応ROIの中心座標の誤差を評価した.正解座標は,画像診断医があらかじめ特定したおおよその腫瘍位置をもとに,比較画像間で腫瘍周辺の画素値の一致度を表すNCC(Normalized Cross-Correlation)を参考に,1pixel単位で筆者らが目視で決定した.
B. 評価結果
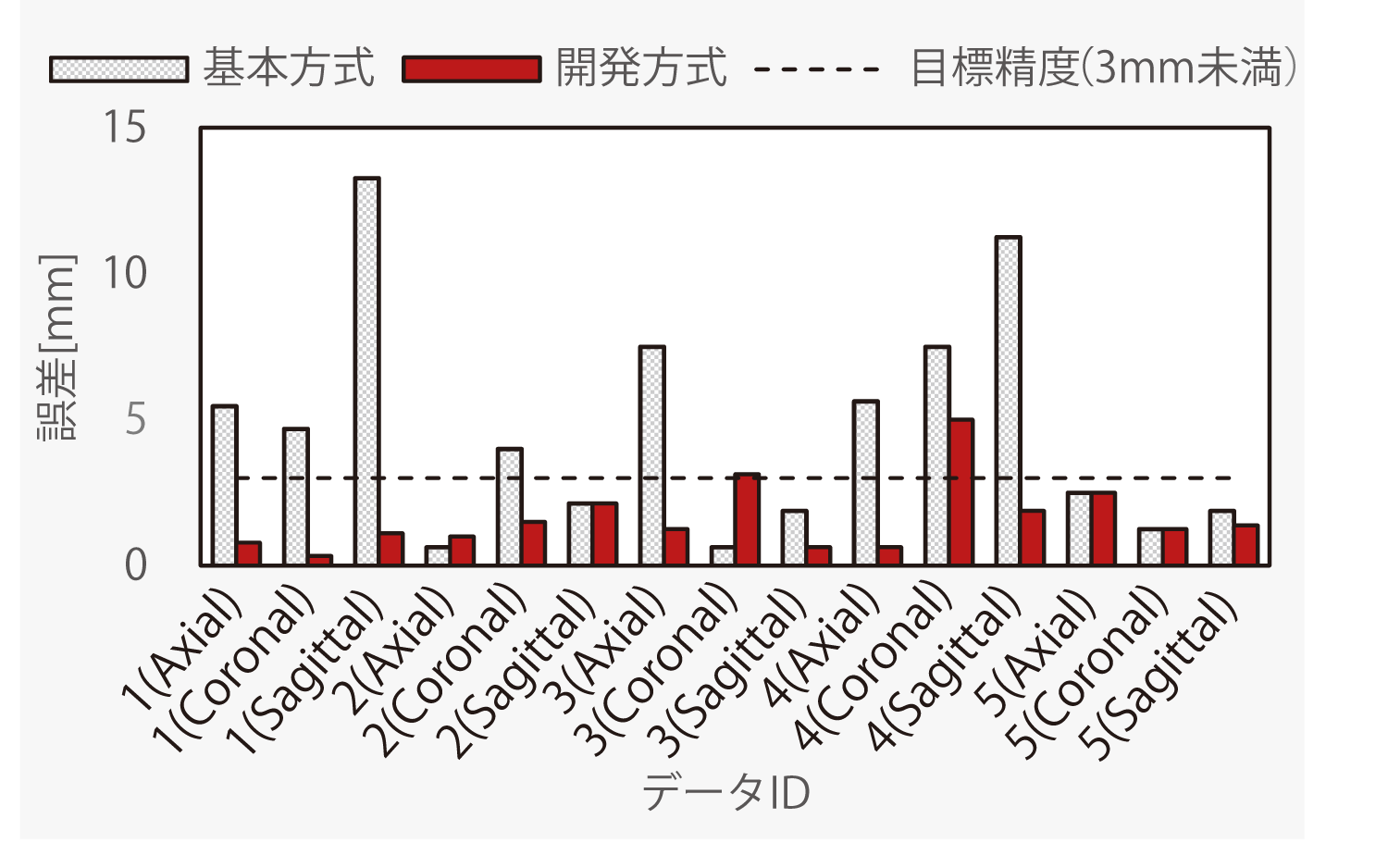
基本方式と開発方式の精度比較を図9に示す.基本方式は,ROI中心から20 pixel刻みで100250 pixel四方の矩形範囲を集計範囲としたときの最小誤差を評価した.実用化の目安となる目標精度3mm未満を達成した症例数は,基本方式は15件中7件(47%)に対し,開発方式は15件中13件(87%)に向上したことを確認した.全症例の平均誤差は,基本方式が約4.7mmに対し,開発方式は約1.6mmであった.
続いて,解像度を1/401/64(縦・横サイズを1/2~1/8)に変更して画像位置合わせの処理時間を計測した.なお,精度は解像度1/4まで変化がないことを確認しており,このときの処理時間は約1.7秒であった.計算機環境はCPUがIntel Xeon CPU E3-1275 V2 (3.5GHz),メモリが8GBであった.高速化の工夫として,全体処理の中で計算コストが高いマッチング処理の実装方法を工夫している.具体的には,バイナリ特徴量を比較する際に用いるハミング距離は,XORの論理演算とビットカウントの組合せで計算できるが,このビットカウント処理をIntel® Core i シリーズ以降のCPUに搭載されたPOPCNT 命令を利用することで数倍の高速化を実現している21).
以上から,開発方式により目標性能である誤差3mm未満,処理時間2秒未満の達成を確認した.
4.2 実証実験
開発した画像位置合わせ機能を試験的に実装したPACSを2016年4月から医療施設にて利用開始した.被験者は3名の画像診断医である.開発した機能の導入前として手動で位置合わせをする期間と,導入後として自動で位置合わせする期間に分けて,比較読影の標準的な症例における作業時間の比較を行った.具体的には,画像位置合わせと比較読影にかかる一症例あたりの平均時間を計測した(表2).

開発機能の導入前,医師B,Cは画像位置合わせ作業と読影作業を同時並行して行っていたため,画像位置合わせ単独の時間計測ができなかった.このため,医師Aのみに着目して画像位置合わせ時間を評価すると,開発機能の導入により約50秒から約3秒への時間短縮を確認した.約2割の画像位置合わせ結果に対し,手動による修正が発生したが,修正時間は平均0.9秒と軽微であった.したがって,修正時間を考慮しても,手動の場合と比べ約9割の時間削減が期待できる.
一方,画像位置合わせ時間を含む比較読影時間に関しては,開発機能の導入前後で統計的な有意差は確認できなかった.これは,画像位置合わせにかかる時間が削減された分,比較読影に多くの時間を割くようになったのではないかと推測される.
画像診断医へのインタビューでは,以前は画像位置合わせ作業により読影中の思考が阻害されていたが,自動化により負荷が軽減し,より集中して業務が行えるようになったとの意見を得ている.処理時間が性能評価時よりも増えている点については,マシンスペックや対象症例の画像枚数の違いなどにより生じたものと推測されるが,同じくインタビューでは,実用上問題ないとの意見を得ている.
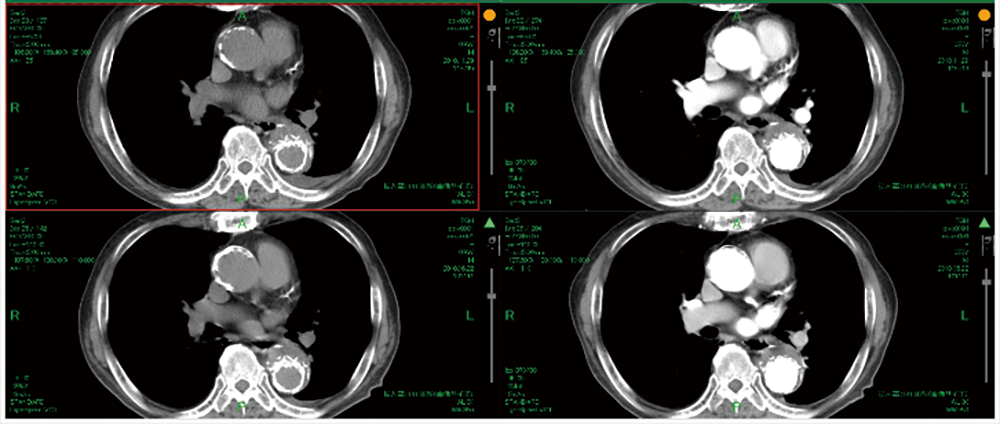
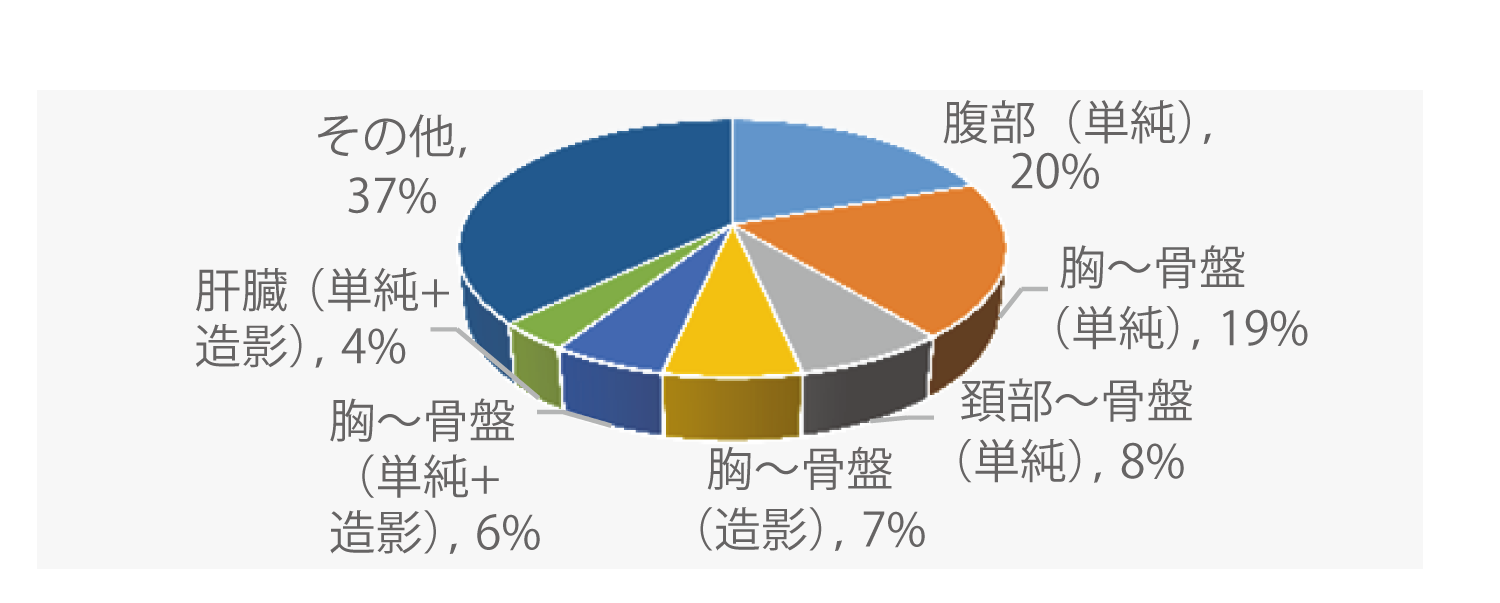
以上,医療現場での実証実験を通して,画像位置合わせ機能による画像診断業務の効率化を示した.新たな知見として,当初の想定よりも幅広い場面で本機能が活用されていることが分かった.たとえば,過去と現在の2組の画像比較だけでなく,異なる種類の検査(造影と非造影,CTとMRI等)の画像比較も同時に行っていることが分かった(図10).また,本機能が利用された画像の撮影部位(図11)を見ると,胸部を含む部位が最も多かった点は想定通りだったが,頚部や肝臓を含む腹部でも利用されていた.ただし,腹部は胸部に比べ,コントラストが低いため十分な数の特徴点が抽出できず,精度が低いことが確認されており,今後の課題として残る.
5.医用画像を扱う際のポイント
これから医用画像解析の技術開発を始める読者に向けた参考情報として,医用画像を扱う上で特に必要となる知識や考え方について紹介する.
5.1 要件定義の考え方
第2章では,画像位置合わせ機能の開発事例を通して,法令やガイドラインなどを踏まえた要件定義の考え方を説明した.再度,以下に箇条書きでまとめた.なお,これは画像位置合わせ機能に限ったものではなく,医療情報システムに関連する技術開発であれば,共通に必要となる考え方である.
①法令・ガイドラインを根拠にした要件
- 腫瘍径6mm以上(CT検診ガイドライン)
- 2秒未満(見読性)
- 可逆圧縮(真正性)
- 保管年数2年以上(保存性,経過観察期間)
②運用環境(PACS)を想定した要件
- 中間データの利用不可(ストレージ容量制約)
③最悪ケース(安全重視)を想定した要件
- 許容誤差3mm未満 (人手で容易に修正可能)
5.2 ツール・開発知識について
CT画像等の医用画像標準規格であるDICOM(Digital Imaging and COmmunication in Medicine)の付帯情報や画素データにアクセスするには,専用のライブラリが必要となる.たとえば,C/C++プログラム向けにはDCMTK22)が有名である.一方で,アルゴリズムの検討段階や手軽にDICOMの中身を確認したい場合には,YAKAMI DICOM Tools23),ImageJ24), OsiriX25)等のフリーウェアが有用である.特にCT画像等は16bitグレースケール画像であるため,まずはこれらビューアソフトを利用して,8bitグレースケール画像(JPEG等)へ変換出力しておけば,一般的な画像処理プログラムでも解析できる.ただし,ビューアは各画像の記録時のコントラスト設定(Window Level / Width)を既定値として変換出力することが多いため注意が必要である.
医用画像解析の性能は,撮影系自体の変化(たとえば,異なるCT装置),撮影時の諸条件(たとえば,線量),撮影後の諸条件(たとえば,複数スライスに画像再構成する間隔)の影響を受けることが知られている26).したがって,これら変動要因に関するDICOM付帯情報を参照し,同一条件のデータのみを解析対象としたり,前処理により可能な限り条件を揃える工夫が重要となる.たとえば,複数スライスからなるCT画像を3次元ボリュームデータに再構成する場合,前記諸条件の1つである画素間隔やスライス間隔の違いは事前に吸収しておきたい.そこで,1ボクセルあたりのx,y,z各方向の実寸を統一するボクセル等方化をしておくことで,異なるパラメータのCT画像間でも同一座標系で処理ができる.
6.おわりに
異なる日時に撮影された同一人物の複数画像間で,呼吸等による位置ずれを補正し,画像比較を容易にする画像位置合わせ機能を開発した.本機能により,経過観察などの比較読影の際に画像位置合わせにかかる時間を低減し,医師の画像診断業務の効率化につながることを確認した.最後に,本稿がこれから医用画像を扱う読者の一助となり,医療のさらなる発展に微力ながら貢献できれば幸いである.
謝辞 実験にご協力いただいた旭川赤十字病院放射線科の峯田昌之先生,長沢研一先生,髙田陽子先生に深謝いたします.
参考文献
- 1)中島康雄,山田 惠,今村惠子,小林和子:諸外国における放射線科医の実態調査,CR News, No.161, pp.12-13 (2007).
- 2)OECD Health Statistics 2016, http://www.oecd.org/els/health-systems/health-data.htm (2017年1月27日現在)
- 3) 厚生労働省:平成27年社会医療診療行為別統計(2016年6月).
- 4)加野亜紀子:健康を守るマンモグラフィ診断支援,情報処理,Vol.51, No.12, pp.1562-1568 (Dec. 2010).
- 5)仁木 登:肺がんCT検診におけるCADの臨床運用,日本放射線技術学会近畿支部会雑誌,Vol.11, No.1, pp.37-41 (2005).
- 6)佐藤佳州,小塚和紀,清野正樹:Deep Learningによる肺CT画像の判別,第16回画像の認識・理解シンポジウム (2013).
- 7)伊藤貴佳,平野 靖,木戸尚治:Deep Learningによる肺結節の良悪性鑑別,第35回日本医用画像工学会大会予稿集,PP-36 (2016).
- 8)陳 斌,古川大介,関口博之,酒井晃二,久保 武,八上全弘,藤本晃司,坂本 亮,江本 豊,川岸将実,青山岳人,飯塚義夫,中込啓太,山本裕之,清水昭伸,富樫かおり:機械学習に基づく胸部CT画像からの肺結節画像所見自動導出に関する検討,第35回日本医用画像工学会大会予稿集,PP-34 (2016).
- 9)Endo, M., Aramaki, T., Asakura, K., Moriguchi, M., Akimaru, M., Osawa, A., Hisanaga, R., Moriya, Y., Shimura, K., Furukawa, H. and Yamaguchi, K. : Content-based Image-retrieval System in Chest Computed Tomography for a Solitary Pulmonary Nodule: Method and Preliminary Experiments, International Journal of Computer Assisted Radiology and Surgery March 2012, Volume 7, Issue 2, pp.331-338 (2012).
- 10) 小塚和紀,高田和豊,近藤堅司,清野正樹,田中雅人,坂井豊彦,木村浩彦:多様な肺疾患の診断・教育を支える類似症例検索技術の開発,電子情報通信学会技術研究報告,Vol.113, No.410, pp.139-142 (2014).
- 11) 山下洋平,徐 睿,平野 靖,木戸尚治,形部倫子,本多 修,富山憲幸:3次元胸部CT画像を用いたびまん性肺疾患に対する類似画像検索,電子情報通信学会技術研究報告,Vol.113, No.410, pp.361-364 (2014).
- 12) 谷口敦司,岡崎智也,青柳康太:画像領域分割技術を用いたCT画像での肺結節の自動体積計測,東芝レビュー,Vol.70, No.8, pp.33-36 (2015).
- 13)(株)シード・プランニング:診断支援ソフトウェアの現状と今後の方向性─薬事法改正で広がる単体ソフトウェア,モバイルメディカルアプリ市場─.
- 14)日本CT検診学会:低線量CTによる肺がん検診の肺結節の判定基準と経過観察の考え方(第4版)(2016年11月).
- 15)Beyer, F., Zierott, L., Fallenberg, E. M., Juergens, K., Stoeckel, J., Heindel, W. and Wormanns, D. : Comparison of Sensitivity and Reading Time for the Use of Computer Aided Detection (CAD) of Pulmonary Nodules at MDCT as Concurrent or Second Reader, Proc. SPIE 6146, Medical Imaging 2006 : Image Perception, Observer Performance, and Technology Assessment, 614617 (2006).
- 16)厚生省健康政策局長,医薬安全局長,保険局長通知:診療録等の電子媒体による保存について(1999年4月22日).
- 17)厚生労働省:医療情報システムの安全管理に関するガイドライン 4.3版(2016年3月).
- 18)日本放射線技術学会:画像情報の確定に関するガイドライン第2.1版(2014年8月).
- 19)http://www.blackfordanalysis.com/products/blackford-smart-localizer/(2017年1月27日現在)
- 20)石原正樹,松田裕司,杉村昌彦,遠藤 進,馬場孝之,上原祐介:放射状特徴点サンプリングによる医用画像位置合わせ手法,電子情報通信学会技術報告,Vol.114, No.454, pp.37-42 (2015).
- 21)安倍 満,長谷川昂宏,藤吉弘亘:対応点探索のための特徴量表現,信学技報,Vol.115, No.388, PRMU2015-104, pp.53-73 (2015).
- 22)http://dicom.offis.de/dcmtk.php.en(2017年1月27日現在)
- 23)http://www.kuhp.kyoto-u.ac.jp/~diag_rad/intro/tech/dicom_tools.ja.html (2017年1月27日現在).
- 24)https://imagej.nih.gov/ij/ (2017年1月27日現在)
- 25)http://www.osirix-viewer.com/ (2017年1月27日現在)
- 26)藤田広志:肺がんCT検診CADシステムの現状と今後の展望,医学物理,Vol.35, No.2, pp.163-166 (2015).
2007年筑波大学大学院修士課程(コンピュータサイエンス)修了.同年(株)富士通研究所入社.現在,画像認識・検索の研究に従事.上級医療情報技師,医用画像情報専門技師.本会シニア会員.
小澤 亮夫(非会員)ozawa.akio@jp.fujitsu.com1995年電気通信大学電子情報学科卒業.同年富士通(株)入社.現在,医療向けシステムの製品開発に従事.
松田 裕司(正会員)matsuda-yuji@jp.fujitsu.com2013年電気通信大学大学院修士課程(総合情報学)修了.同年(株)富士通研究所入社.現在,画像認識の研究に従事.
杉村 昌彦(正会員)suginy@jp.fujitsu.com1995年京都大学大学院修士課程(応用システム科学)修了.同年(株)富士通研究所入社.現在,画像認識・検索の研究に従事.
武部 浩明(非会員)takebe.hiroaki@jp.fujitsu.com1995年東京大学大学院修士課程(数理科学)修了.同年(株)富士通研究所入社.2014年九州大学大学院博士後期課程単位取得退学.現在,画像認識の研究に従事.博士(工学).
遠藤 進(非会員)endou.susumu-02@jp.fujitsu.com1994年東北大学大学院修士課程(情報工学)修了.同年(株)富士通研究所入社.現在,画像認識・検索の研究に従事.
馬場 孝之(正会員)baba-t@jp.fujitsu.com1998年大阪大学大学院博士課程(情報数理系)修了.1997~1999年日本学術振興会特別研究員.1999年(株)富士通研究所入社.現在,画像・映像検索の研究に従事.博士(工学).
上原 祐介(正会員)yuehara@jp.fujitsu.com1992年名古屋大学大学院博士課程満了.同年(株)富士通研究所入社.現在,画像認識・検索の研究に従事.
採録決定:2017年11月11日
編集担当:伊藤 智(産業技術総合研究所)